最初に覚えたい!古典的Pdカップリング反応7選
始めに
クロスカップリング反応は、有機合成では非常に重要な反応のひとつです。戦後に開発された反応で、多くの日本人が関わっています。マクマリーにはほとんど載っていませんが、研究室では日常的に使用する反応になるので、知っておいて損はありません。
今回は、最初に覚えるべき古典的なPdカップリング反応を7つ紹介します。
(エクスキューズ:査読を受けていないし、私はしがない修士学生なので、間違っている情報が載っている可能性もあるので、その時はごめんなさい。)
クロスカップリングの一般的な反応機構
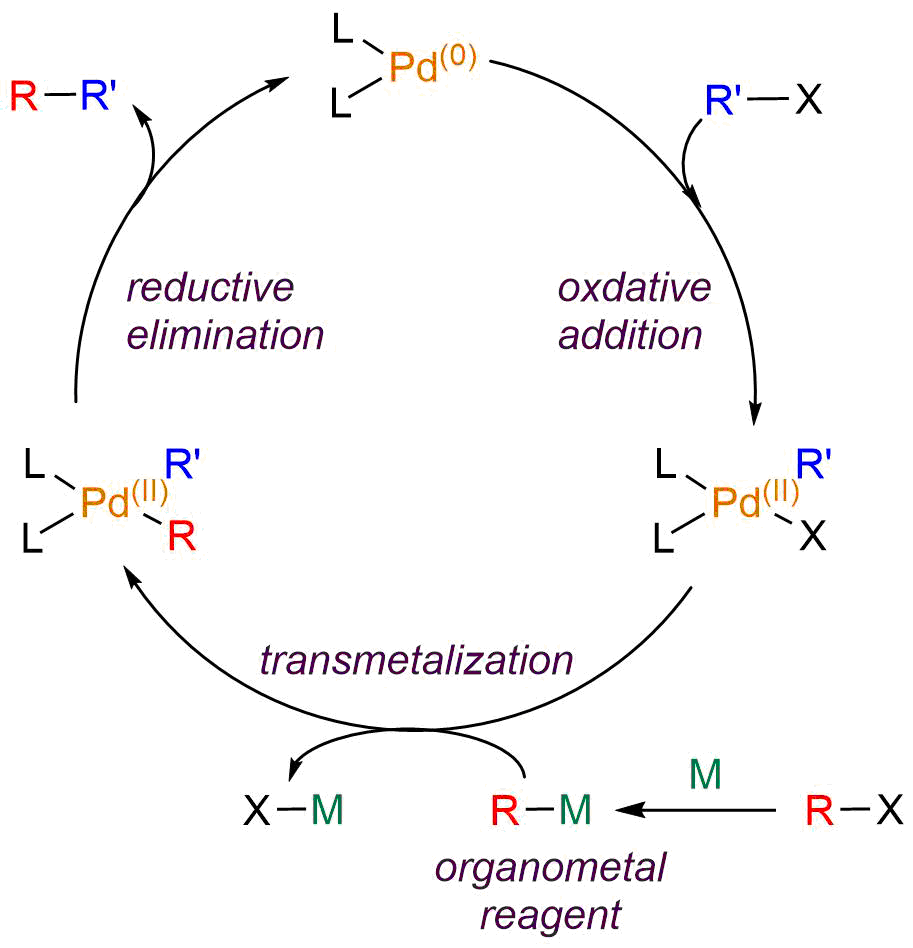
クロス選択的にカップリング反応を進行させるためには、有機ハロゲン化物と有機金属試薬を組み合わせることが一般的です。反応は以下の流れで進行します(下図)。
様々な有機金属試薬を利用したカップリング反応が開発されており、それぞれに人名反応が付いています。以下にひとつずつ紹介します。
1. ビアリール形成反応
1-1. Stille カップリング:スズ
有機スズ化合物 R-SnBu3 とトランスメタル化する反応。
ほぼ中性の穏やかな条件で反応が進行することが利点。天然物合成の最終段階によく登場する。
有機スズ化合物は有毒なのが注意点。
ビニルスズ化合物の利用もよく見る印象。
1-2. 根岸カップリング:亜鉛
亜鉛ソースにはZnCl2が一般的。
後述の熊田カップリングと比較して温和な有機金属試薬のため、副反応などを抑制できる。
アルキル亜鉛化合物も利用可能らしい。
1-3. 熊田カップリング:マグネシウム
有機マグネシウム試薬(グリニャール試薬) RMgBrとトランスメタル化する反応。
反応性が高い。しかしグリニャール試薬と反応する基質は使用できない。
歴史的にクロスカップリング反応の先駆けであり、今でもよく利用される。
1-4. 鈴木―宮浦カップリング:ホウ素(ボレート)
ボロン酸 R-B(OH)2と塩基からなるボレートとトランスメタル化する反応。
ボロン酸そのものでなく、そこに塩基を加えたボレートが活性種であることに注意。
ボロン酸が安定で容易に調整でき、塩基を加えるだけで反応が進行することが利点。
ただし塩基不安定な基質は利用が難しい。
ビアリール形成のファーストチョイスは鈴木宮浦反応と言っていいくらい、メジャーな反応。
1-5. 檜山カップリング:ケイ素(シリケート)
有機ケイ素試薬 R-Si(OR)3 とフッ素などの強いLewis塩基とからなる、有機シリケート種とトランスメタル化する反応。鈴木宮浦カップリングのケイ素版。
大きなマイナスポイントとして、ケイ素の置換基にはヘテロ原子やアリール基が通常必須となる。トリアルキルシリル基の場合にはシリケート種の形成が困難。現時点ではヘテロ原子置換ケイ素化合物の穏和で一般的な合成法に乏しく、鈴木宮浦カップリングほど応用展開が進んでいない。
*実際、この反応は私も今回このブログを書くにあたり始めてきちんと認知した。他の反応と比較してマイナーな印象はある。
以上が一般にビアリール形成に用いられる反応である。
これらの反応は有名で使い勝手がいいために、様々な変法が開発されており、現在ではアリールだけでない様々な基質に展開できる。(私は詳しくは知らない。)
以下は、アリール以外の基質を利用する反応を紹介します。
2. その他の構造形成反応(アルキン、アルケン)
2-1. 薗頭カップリング:アルキン(アルキニル銅)
アルキンとヨウ化銅が反応したアルキニル銅とトランスメタル化する反応。
ヨウ化銅はトランスメタル化の際に再生するため、触媒量でよい。
アルキンの導入といえば薗頭というくらい定番な反応。
2-2. Heck反応:アルケン
Heck反応の反応機構は、これまでの反応とは少し異なり以下のように進行する。
- ハロゲン化アリールの酸化的付加
- アルケンの移動挿入(migratory insertion)反応:パラジウムがアルケンにsyn付加する
- β水素脱離(β-hydride elimination)反応:パラジウムの隣の炭素に結合した水素と、パラジウムがsyn脱離して、アルケンが生成する。
- Pdは2価のままなので、塩基で還元してPd(0)が再生する。
アルケンには電子吸引基(エステルなど)が結合した基質を用いることが多い。位置選択性を制御するためである。電子吸引基が付いていない方の炭素で選択的に反応する。反対にエーテルなどの電子供与基が結合した基質は反応位置の制御が難しい。
(余談だが、オレフィンメタセシスの基質も、電子吸引基を導入した基質はクロス選択性がよい。)
以上、最低限の情報だけ纏めました。
このブログ記事を書こうと思った経緯を一応書いておきます。
私は今ニッケル触媒を利用したハロゲン化アリールのホモカップリング反応(山本カップリング)を少々扱っていまして、その反応の総説をこの間読んだのですね。そこのintroに、パラジウムカップリングの例として上記の7つを挙げていました。せっかくの機会なので一覧にしてまとめたいと思い、記録した次第です。
本当、学部3年生や4年生が勉強するべき内容なのですが、まあいつになっても勉強には遅くないということでね、まあ許してね。
ちなみに、弊研究グループでは薗頭反応と鈴木宮浦反応は日常的に使用します。これにWilliumsonエーテル合成を加えた3反応が、弊グループの化合物の合成でよく使う3種の神器ですね。出来るだけこの反応を利用できるように、構造と合成スキームを設計する。
せっかくなら上記の反応に加えて、Pdカップリングとして有名なBuchwald-Hartwigアミノ化や辻・トロスト反応も追記したかったのですが、もう日付回っていて眠いのでまた今度ね。